A imitação de condições fisiológicas ajuda os pesquisadores a encontrar ligantes de metal
Pesquisadores desenvolveram um método para identificar pequenas moléculas que se ligam a íons metálicos.Os íons metálicos são essenciais na biologia.Mas identificar com quais moléculas – e especialmente com quais pequenas moléculas – esses íons metálicos interagem pode ser um desafio.
Para separar metabólitos para análise, os métodos metabolômicos convencionais usam solventes orgânicos e pHs baixos, o que pode causar a dissociação de complexos metálicos.Pieter C. Dorrestein, da Universidade da Califórnia em San Diego, e colegas de trabalho queriam manter os complexos juntos para análise, imitando as condições nativas encontradas nas células.Mas se eles usassem condições fisiológicas durante a separação de moléculas, eles teriam que reotimizar as condições de separação para cada condição fisiológica que eles queriam testar.
Em vez disso, os pesquisadores desenvolveram uma abordagem de dois estágios que introduz condições fisiológicas entre uma separação cromatográfica convencional e uma análise espectrométrica de massa (Nat. Chem. 2021, DOI: 10.1038/s41557-021-00803-1).Primeiro, eles separaram um extrato biológico usando cromatografia líquida de alta eficiência convencional.Em seguida, eles ajustaram o pH do fluxo que sai da coluna cromatográfica para imitar as condições fisiológicas, adicionaram íons metálicos e analisaram a mistura com espectrometria de massa.Eles executaram a análise duas vezes para obter espectros de massa de pequenas moléculas com e sem metais.Para identificar quais moléculas ligam metais, eles usaram um método computacional que usa formas de pico para inferir conexões entre os espectros de versões ligadas e não ligadas.
Uma maneira de imitar ainda mais as condições fisiológicas, diz Dorrestein, seria adicionar altas concentrações de íons, como sódio ou potássio, e baixas concentrações do metal de interesse.“Isso se torna um experimento de competição.Ele basicamente dirá a você, OK, essa molécula nessas condições tem mais propensão a se ligar ao sódio e ao potássio ou a esse metal único que você adicionou”, diz Dorrestein.“Podemos infundir muitos metais diferentes simultaneamente e podemos realmente entender a preferência e a seletividade nesse contexto”.
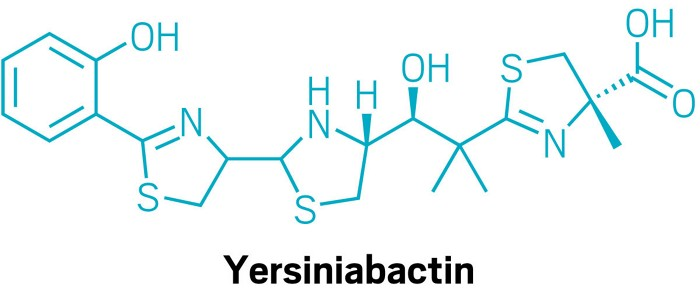
Em extratos de cultura de Escherichia coli, os pesquisadores identificaram compostos conhecidos de ligação de ferro, como yersiniabactina e aerobactina.No caso da yersiniabactina, eles descobriram que ela também pode se ligar ao zinco.
Os pesquisadores identificaram compostos de ligação a metais em amostras tão complexas quanto a matéria orgânica dissolvida do oceano.“Essa é absolutamente uma das amostras mais complexas que já vi”, diz Dorrestein.“Provavelmente é tão complexo quanto, se não mais complexo, do que o petróleo bruto.”O método identificou o ácido domóico como uma molécula de ligação ao cobre e sugeriu que ele se liga ao Cu2+ como um dímero.
“Uma abordagem ômica para identificar todos os metabólitos de ligação a metais em uma amostra é extremamente útil devido à importância da quelação biológica de metais”, escreve Oliver Baars, que estuda metabólitos de ligação a metais produzidos por plantas e micróbios na North Carolina State University. o email.
“Dorrestein e colegas de trabalho fornecem um ensaio elegante e muito necessário para investigar melhor qual poderia ser o papel fisiológico dos íons metálicos na célula”, escreve Albert JR Heck, pioneiro em análises de espectrometria de massa nativa na Universidade de Utrecht, por e-mail.“Um possível próximo passo seria extrair os metabólitos sob condições nativas da célula e fracioná-los também sob condições nativas, para ver quais metabólitos carregam quais íons metálicos celulares endógenos”.
Notícias de química e engenharia
ISSN 0009-2347
Direitos autorais © 2021 American Chemical Society
Horário da postagem: 23 de dezembro de 2021

